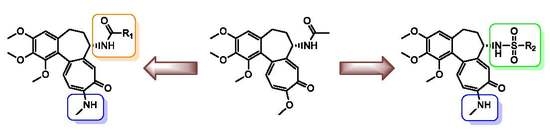
To już trzecia publikacja naukowa, która powstała w ramach doktoratu wdrożeniowego Julii Krzywik pracującej w firmie TRIMEN CHEMICALS z Łodzi. W pracy opisano syntezę nowych karbaminianowych i tiokarbaminianowych pochodnych 10-demetoksy-10-metyloaminokolchicyny oraz szczegółowe badania krystalograficzne i strukturalne 4 spośród otrzymanych związków.


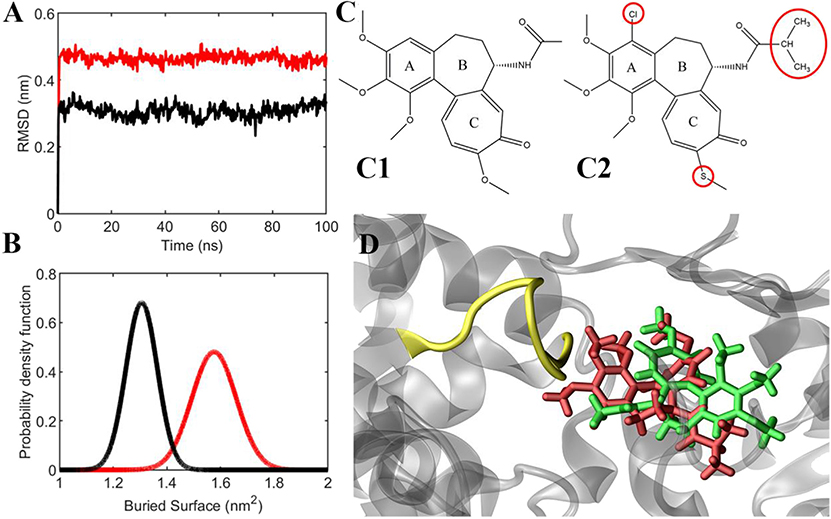
Wszystkie pochodne kolchicyny zostały przetestowane pod kątem ich aktywności przeciwproliferacyjnej wobec czterech linii komórkowych ludzkich nowotworów. Większość badanych związków wykazywała większą cytotoksyczność i charakteryzowała się wyższym współczynnikiem selektywności od standardowych leków przeciwnowotworowych, takich jak cisplatyna i doksorubicyna oraz od niezmodyfikowanej kolchicyny. Badania dokowania molekularnego potwierdziły zdolność otrzymanych związków do wiązania się z kolchicynowym miejscem wiążącym w tubulinie (ang. colchicine binding site , CBS).

Julia Krzywik, Maral Aminpour, Jan Janczak, Ewa Maj, Mahshad Moshari, Witold Mozga, Joanna Wietrzyk, Jack. A. Tuszyński, Adam Huczyński, ”An insight into the anticancer potential of carbamates and thiocarbamates of 10-demethoxy-10-methylaminocolchicine”, (2021), European Journal of Medicinal Chemistry, 113282.