| Minister Nauki i Szkolnictwa Wyższego rozstrzygnął dziewiąty konkurs w ramach programu Diamentowy Grant na finansowanie projektów dla wybitnie uzdolnionych studentów prowadzących badania naukowe na wysokim poziomie i posiadających wyróżniający się dorobek naukowy. Tegorocznym laureatem został Michał Sulik – student współpracujący z grupą Prof. Adama Huczyńskiego. Na realizację swojego projektu zatytułowanego „Synteza oraz badania właściwości przeciwnowotworowych i przeciwpasożytniczych nowych pochodnych iwermektyny” otrzymał on kwotę 220 tysięcy złotych. Michałowi gratulujemy i życzymy powodzeniach w syntezach. Iwermektyna (IWR) to związek wykazujący niezwykle szerokie spektrum aktywności przeciwpasożytniczej, dzięki czemu znalazł on powszechne zastosowanie w leczeniu najróżniejszych chorób, między innymi ślepoty rzecznej (onchocerkozy), słoniowacizny, węgorczycy, świerzbu oraz wszawicy. Stosowanie IWR od 1987 roku znacząco poprawiło nie tylko jakość życia ludzi w krajach Afryki Subsaharyjskiej, Indiach i wielu innych, ale również umożliwiło leczenie chorób, które wcześniej niosły pewną śmierć. Za odkrycie oraz badania nad iwermektyną przyznana została Nagroda Nobla w 2015 roku w dziedzinie fizjologii/medycyny. IWR dzięki swojej skuteczności, wszechstronności oraz bezpieczeństwu stosowania tak znacząco wpłynęła na świat medycyny, że wielu naukowców określa ją mianem „wonder drug” (cudowny lek), przyrównując ją chociażby do aspiryny czy penicyliny. Poza aktywnością wobec pasożytów, w ostatnich latach pojawia się coraz więcej artykułów naukowych traktujących o niezwykle interesującej aktywności przeciwnowotworowej IWR, w tym wobec lekoopornych oraz macierzystych komórek nowotworowych. Ostatnie badania wykazało, że iwermektyna jest inhibitorem wirusa wywołującego COVID-19 (SARS-CoV-2). Jednokrotne podanie leku umożliwiająca około 5000-krotną redukcję wirusa w hodowli komórkowej już po 48 godzinach. |
Dominika Czerwonka – została laureatką w konkursie ETIUDA 8
Narodowe Centrum Nauki ogłosiło wyniki ósmej edycji konkursu ETIUDA. Laureatką tej edycji konkursu została mgr Dominika Czerwonka. Rywalizacja była bardzo duża, gdyż wnioski złożyło aż 448 młodych doktorantów i doktorantek, a finansowanie przyznano tylko 84 z nich. W ramach stypendium Dominika Czerwonka odbędzie również 3 miesięczny naukowy w zespole naukowym Prof. Raphaëla Rodrigueza w Instytucie Curie w Paryżu. Dominice gratulujemy i życzymy wytrwałości w realizacji projektu.
Artykuł o dimerach antybiotyków jonoforowych ukazał się w Biomolceules
W naszym artykule opisaliśmy syntezę serii oryginalnych homo- i heterodimerów jonoforów, w których dwie cząsteczki salinomycyny zostały połączone za pomocą łączników triazolowych oraz takie, w których salinomycyna jest połączona z kwasem lasalowym, monenzyną lub kwasem betulinowym tworząc „mieszane” struktury dimeryczne. Otrzymane dimery wykazały niezwykle ciekawe właściwości przeciwnowotworowe.
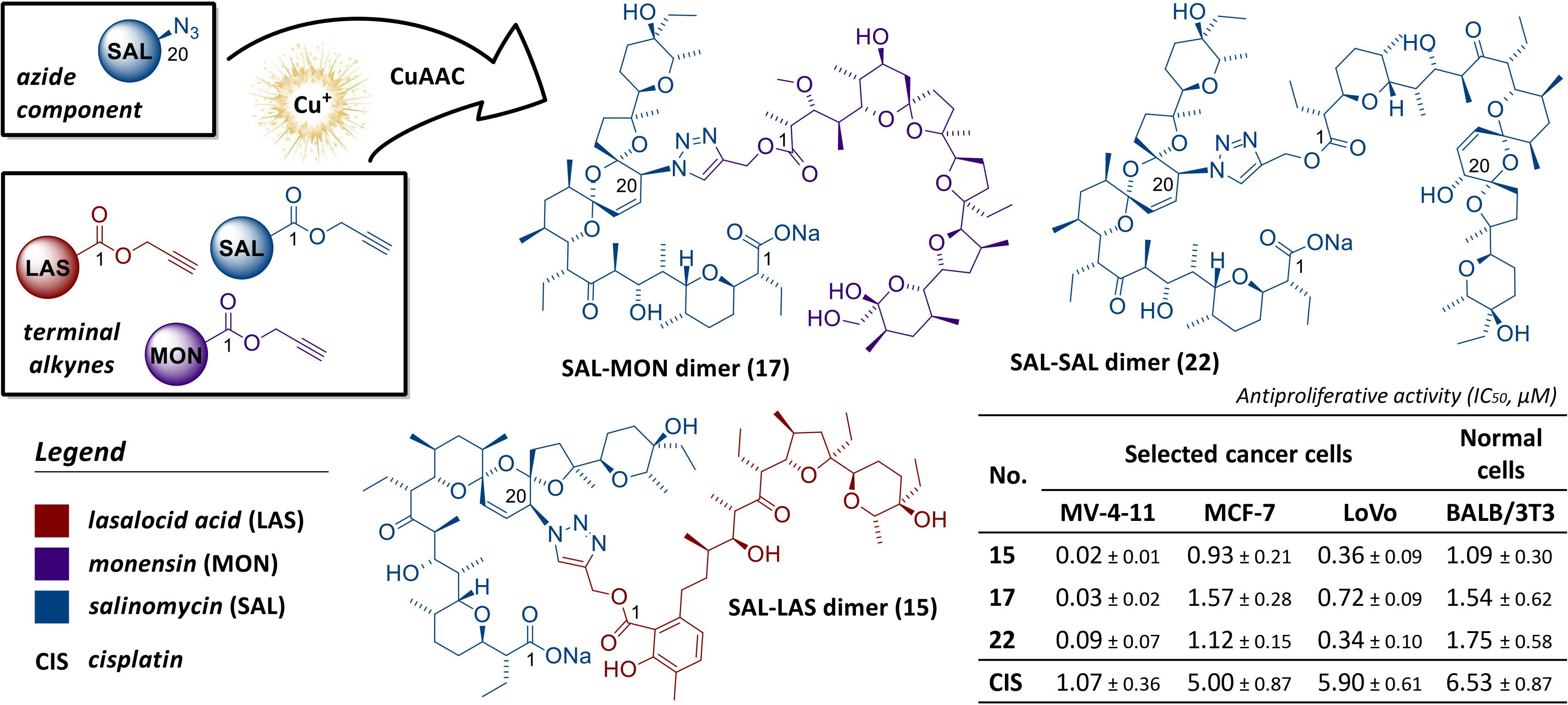
Michał Sulik, Ewa Maj, Joanna Wietrzyk, Adam Huczyński, Michał Antoszczak, „Synthesis and Anticancer Activity of Dimeric Polyether Ionophores”, Biomolecules 2020, 10, 1039.
Dr Michał Antoszczak – laureatem stypendium dla wybitnych młodych naukowców
Minister Nauki i Szkolnictwa Wyższego przyznał stypendium dla wybitnych młodych naukowców. Laureatem tego prestiżowego stypendium został adiunkt w Zakładzie Chemii Medycznej – dr Michał Antoszczak.
Michałowi serdecznie gratulujemy i życzymy dalszych sukcesów.
Publikacja na temat przeciwnowotworowych właściwości nowych pochodnych kolchicyny ukazała się w Molecules.
Z przyjemnością informujemy, że w MOLECULES ukazała się pierwsza praca będąca efektem współpracy pomiędzy przemysłem (firma TriMen Chemicals z Łodzi) a naukowcami z rożnych ośrodków naukowych. Publikacja jest wynikiem badań prowadzonych w ramach realizacji doktoratu wdrożeniowego Julii Krzywik.
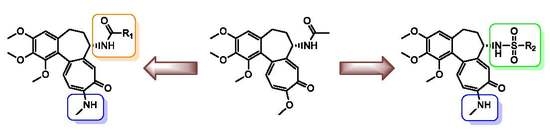
Julia Krzywik, Witold Mozga, Maral Aminpour, Jan Janczak, Ewa Maj, Joanna Wietrzyk, Jack A. Tuszyński, Adam Huczyński, „Synthesis, Antiproliferative Activity and Molecular Docking Studies of Novel Doubly Modified Colchicine Amides and Sulfonamides as Anticancer Agents” (2020) Molecules, 25(8), 1789.
Kolchicyna – nowa nadzieja na lek zwalczający COVID-19?
W badaniu klinicznym o nazwie COLCORONA kolchicyna jest stosowana w celu zmniejszenia nadmiernej reakcji zapalnej wywołanej przez koronawirus. Reakcja zapalna prowadzić może do zespołu ostrej niewydolności oddechowej (ARDS), niewydolności narządów i śmierci. U niektórych osób zarażonych koronawirusem reakcja układu odpornościowego nazywana „burzą cytokin” powoduje powstanie zbyt wielu przekaźników odpornościowych. Oznacza to, że główne części ciała stają się bardzo zaognione i nie mogą prawidłowo działać. Płuca powoli wypełniają się, co powoduje poważne problemy z oddychaniem i zapalenie płuc. Serce, wątroba i nerki również mogą ulec zapaleniu, co może prowadzić do poważnych powikłań, a nawet niewydolności narządów i śmierci. Kolchicyna będzie stosowana ze względu na jej znane działanie przeciwzapalne. Zmniejszając nadmierne stany zapalne podczas leczenia COVID-19 lekarze z Montreal Heart Institute mają nadzieję, że u chorych leczonych kolchicyną układ odpornościowy organizmu będzie w stanie walczyć z koronawirusem i zmniejszy się liczba powikłań takich jak zapalenia płuc oraz niewydolność narządów, co pozwoli uchronić pacjentów od śmierci.
https://clinicaltrials.gov/ct2/show/NCT04322682
Również naukowcy z National and Kapodistrian University of Athens planują użyć kolchicyny w klinicznych badaniach skupionych na leczeniu chorych na COVID-19.
https://clinicaltrials.gov/ct2/show/NCT04326790
Koronawirus COVID-19 – publikacje naszego współpracownika z University of Alberta
Koronawirus wywołujący chorobę COVID-19 (ang. corona-virus-disease-2019 – choroba koronawirusowa z 2019 roku) jest obecnie obiektem bardzo intensywnych badań. Pierwszy przypadeki COVID-19 zanotowano w chińskim mieście Wuhan, a obecnie infekcje wykrywane są w Polsce i na całym świecie. Wirus ten jest przyczyną ciężkiej niewydolności oddechowej i jest śmiertelnym zagrożeniem, zwłaszcza dla starszych ludzi.
Prof. Jack Tuszynski, z którym od lat współpracujemy, wraz ze swoimi współpracownikami opublikował niedawno dwie publikacje, które są szybką odpowiedzią na brak leków na koronawirusa. Zainteresowanym polecamy artykuły, a profesorowi Tuszynskiemu i współpracownikom szczerze gratulujemy.
Maria Bzówka, Karolina Mitusińska, Agata Raczyńska, Aleksandra Samol, Jack Tuszyński, Artur Góra, „Molecular Dynamics Simulations Indicate the COVID-19 Mpro Is Not a Viable Target for Small-Molecule Inhibitors Design” bioRxiv 2020.02.27.968008
Sahu, K.; Noskov, S.; Tuszynski, J.; Houghton, M.; Tyrrell, D.L. Computational Screening of Molecules Approved in Phase-I Clinical Trials to Identify 3CL Protease Inhibitors to Treat COVID-19. Preprints 2020, 2020040015

Artykuł opisujący aktywność in vitro i ex vivo pochodnych kolchicyny ukazał się Journal of Biochemical and Molecular Toxicology
W wyniku kontynuowania współpracy z naukowcami z USA (Department of Biochemistry and Molecular Biology, University of Arkansas for Medical Sciences) przebadano serię 17 wybranych N-karbaminianowych pochodnych N-deacetylo-4-(bromo/chloro/jodo)tiokolchicyny na dwóch typach pierwotnych komórek nowotworowych obejmujących ostrą limfoblastyczną białaczkę (ALL) i ludzki nowotwór piersi (BC) pochodzące z dwóch różnych podtypów nowotworów, ER+ inwazyjny rak stopnia III (IDCG3) i rak z przerzutami (MC). Cztery z pochodnych kolchicyny były bardziej aktywne od związku wyjściowego w zakresie nanomolowych stężeń. Dodatkowo kilka otrzymanych pochodnych kolchicyny działało selektywnie na pierwotne komórki raka piersi w porównaniu do normalnego nabłonka piersi. Najbardziej obiecujące pochodne zostały następnie przetestowane na panelu NCI-60 (National Cancer Institute, USA) wobec aż 60 ludzkich nowotworowych linii komórkowych. Tak szeroko zakrojone badania przesiewowe pokazały, iż siedem spośród testowanych pochodnych kolchicyny miało silniejsze działanie cytotoksyczne od niemodyfikowanej kolchicyny m.in. przeciwko białaczce, niedrobnokomórkowemu nowotworowi płuc, a także nowotworom jelita grubego i prostaty. Dodatkowo kolchicynę i dwie najbardziej aktywne pochodne przebadano na aktywność ex vivo na uzyskanych od chorych pacjentów wycinkach przerzutowego nowotworu piersi (pobranych z wycinków pooperacyjnych). Uzyskane wyniki potwierdziły niezwykle wysoki potencjał przeciwnowotworowy nowych podwójnie i potrójnie zmodyfikowanych uretanów kolchicyny i tiokolchicyny.
Alicja Urbaniak, Fariba Jousheghany, Sergio Piña‐Oviedo, Youzhong Yuan, Urszula Majcher‐Uchańska, Greta Klejborowska, Anika Moorjani, Behjatolah Monzavi‐Karbassi, Adam Huczyński, Timothy C. Chambers, „Carbamate derivatives of colchicine show potent activity towards primary acute lymphoblastic leukemia and primary breast cancer cells – in vitro and ex vivo study”, J. Biochem. Mol. Toxicol., 2020;e22487. https://doi.org/10.1002/jbt.22487
Publikacja na temat nowych pochodnych kolchicyny ukazała się w MOLECULES
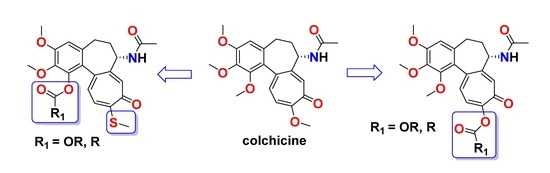
Dominika Czerwonka, Szymon Sobczak, Ewa Maj, Joanna Wietrzyk, Andrzej Katrusiak, Adam Huczyński, „Synthesis and Antiproliferative Screening Of Novel Analogs of Regioselectively Demethylated Colchicine and Thiocolchicine” Molecules, 2020, 25, 1180.
Artykuł w Bioorganic & Medicinal Chemistry Letters opisujący aktywność przeciwbakteryjną pochodnych salinomycyny

Wraz z zespołem dr hab. Joanny Stefańskiej z Zakładu Mikrobiologii Farmaceutycznej WUM opublikowaliśmy nową pracę dotyczącą podwójnie modyfikowanych pochodnych salinomycyny. Są one aktywne wobec antybiotykoopornych szczepów gronkowców: Staphylococcus aureus and Staphylococcus epidermidis.
Michał Sulik, Karolina Stępień, Joanna Stefańska, Adam Huczyński, Michał Antoszczak, „Antibacterial activity of singly and doubly modified salinomycin derivatives”, Bioorganic & Medicinal Chemistry Letters, 2020, 127062,
Stypendia w programie im. Bekkera przyznane!
Narodowa Agencja Wymiany Akademickiej (NAWA) po raz drugi ufundowała stypendia pokrywające koszty pobytu w renomowanych ośrodkach naukowych za granicą. Wśród 126 laureatów programu stypendialnego im. Bekkera znalazło się również kilku naukowców z naszego Wydziału, w tym Dr Michał Antoszczak – adiunkt w Zakładzie Chemii Medycznej.
W ramach stypendium Dr Michał Antoszczak odbędzie 12-miesięczny staż naukowy w zespole naukowym Prof. Raphaëla Rodrigueza w Instytucie Curie w Paryżu, w trakcie którego będzie miał możliwość prowadzenia innowacyjnych badań dotyczących syntezy nowych kandydatów na leki onkologiczne. Niewątpliwą zaletą stażu będzie również możliwość odbycia przez Pana Doktora szeregu szkoleń oraz własnoręcznego wykonania serii zaawansowanych badań biologicznych zsyntezowanych po raz pierwszy związków chemicznych, w tym tych na macierzystych komórkach nowotworowych.
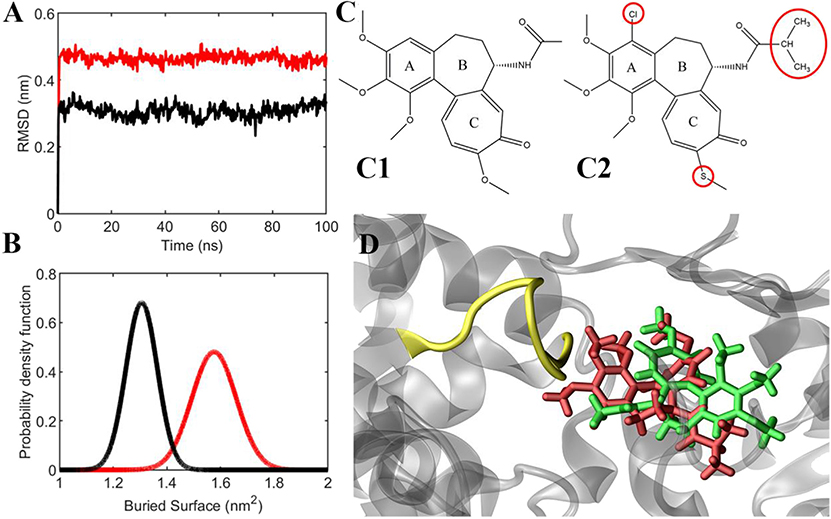
In Silico Methods for Drug Design and Discovery – nowa publikacja z zespołem profesora Jacka Tuszynskiego
Lorenzo Pallante , Antonio Rocca , Greta Klejborowska, Adam Huczyński , Gianvito Grasso , Jack Adam Tuszynski and Marco Agostino Deriu, „In silico Investigations of the Mode of Action of Novel Colchicine Derivatives Targeting β-Tubulin Isotypes: A Search for a Selective and Specific βIII Tubulin Ligand” Front. Chem., 2020, 8, 108
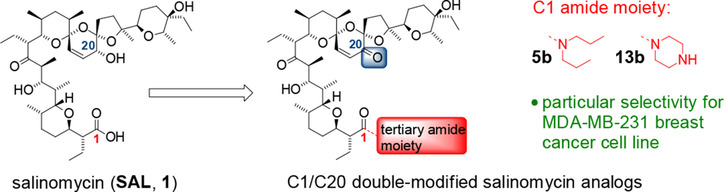
Publikacja w ChemMedChem – aktywność przeciwnowotworowa podwójnie modyfikowanych pochodnych salinomycyny
Dominika Czerwonka, Alicja Urbaniak, Szymon Sobczak, Sergio Piña‐Oviedo, Timothy C. Chambers, Michał Antoszczak, Adam Huczyński, „Synthesis and Anticancer Activity of Tertiary Amides of Salinomycin and Their C20‐oxo Analogues” ChemMedChem, 2020, 15, 236-246.
https://onlinelibrary.wiley.com/doi/full/10.1002/cmdc.201900593
Nowa aktywność salinomycyny i jej pochodnych- publikacja w International Journal of Oncology
Tariq Alqahtani Vishnu, Muthuraj Kumarasamy, Adam Huczyński, Daekyu Sun, „Salinomycin and its derivatives as potent RET transcriptional inhibitors for the treatment of medullary thyroid carcinoma”, International Journal of Oncology, 2020 Jan;56(1):348-358
Aktywność przeciwnowotworowa nowych pochodnych kolchicyny – publikacja w Chem. Biol. Drug Des.
Greta Klejborowska, Mahshad Moshari, Ewa Maj, Urszula Majcher, Jordane Preto, Joanna Wietrzyk, Jack A Tuszynski, Adam Huczyński, „Synthesis, antiproliferative activity, and molecular docking studies of 4‐chlorothiocolchicine analogues”, Chem. Biol. Drug Des. 2020 Jan;95(1):182-191
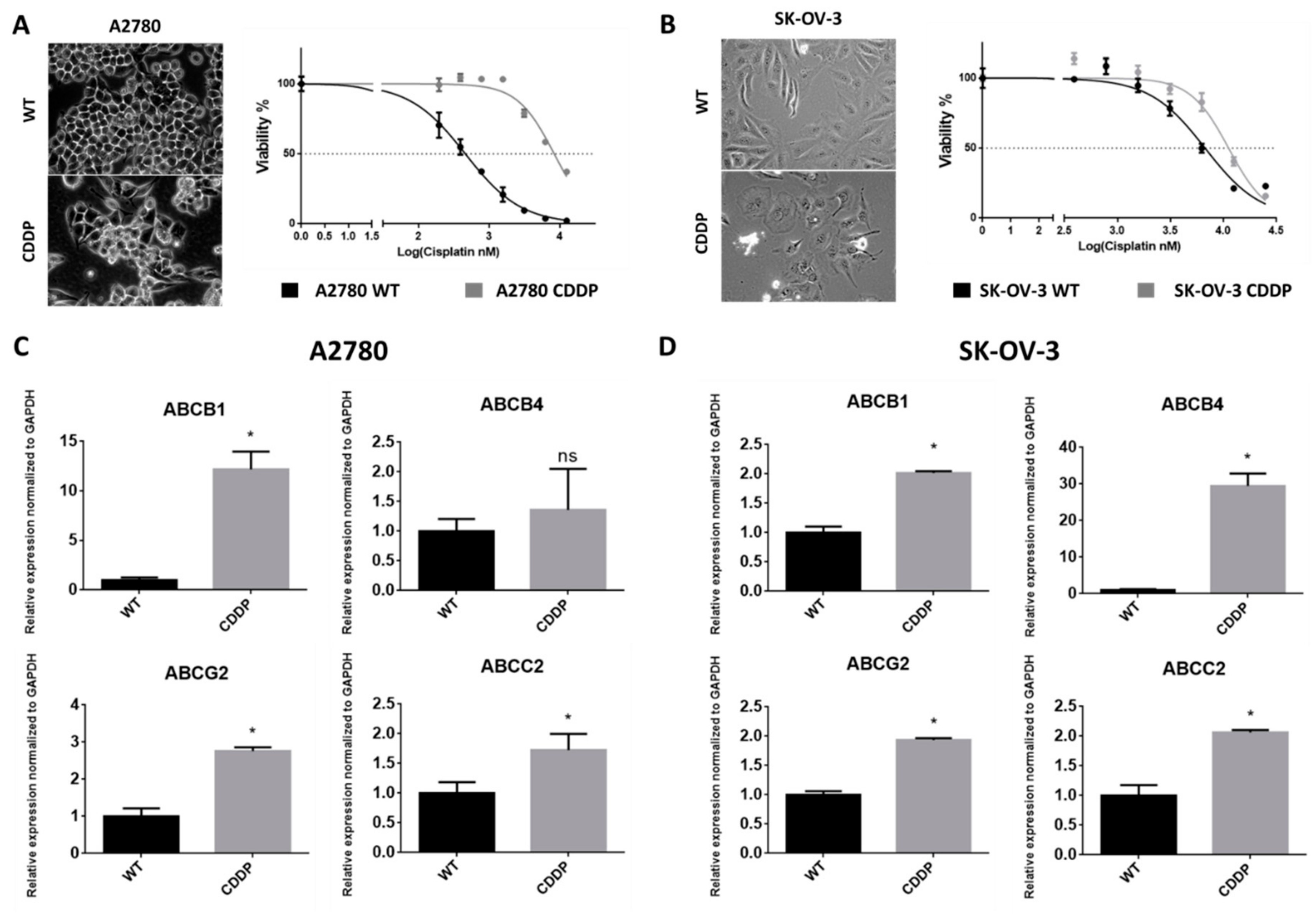
Nowa publikacja na temat aktywności salinomycyny wobec lekoopornych linii nowotworu jajnika
Michalak, Marcin; Lach, Michał S.; Antoszczak, Michał; Huczyński, Adam; Suchorska, Wiktoria M. „Overcoming Resistance to Platinum-Based Drugs in Ovarian Cancer by Salinomycin and Its Derivatives—An In Vitro Study.”
Molecules, 2020, 25, no. 3: 537
Nowa praca na temat modyfikacji kolchicyny
Greta Klejborowska, Alicja Urbaniak, Ewa Maj, Jordane Preto, Mahshad Moshari, Joanna Wietrzyk, Jack A. Tuszynski, Timothy C. Chambers, Adam Huczyński,
„Synthesis, biological evaluation and molecular docking studies of new amides of 4-chlorothiocolchicine as anticancer agents”, Bioorganic Chemistry, 2020, 97, 103664,


Publikacja w European Journal of Pharmacology
Nowa publikacja przeglądowa: Michał Antoszczak, Anna Markowska, Janina Markowska, Adam Huczyński, „Old wine in new bottles: Drug repurposing in oncology”
European Journal of Pharmacology, Volume 866, 2020, 172784,


Zakład Chemii Medycznej
Zakład Chemii Medycznej jest nowym Zakładem w strukturach Wydziału Chemii UAM. Został utworzony 1 stycznia 2020 roku, a na jego kierownika powołano prof. dr hab. Adama Huczyńskiego.
